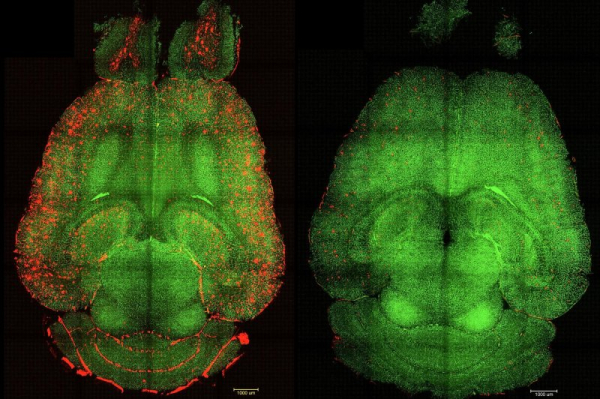
Hiszpańscy i chińscy naukowcy poinformowali w poniedziałek, że użyli specjalnie dostosowanych nanocząsteczek, aby usunąć z mózgów myszy nagromadzone toksyny, która jest kluczowa dla choroby Alzheimera.
Naukowcy z Instytutu Bioinżynierii Katalonii w Barcelonie w Hiszpanii oraz Szpitala Zachodnich Chin przy Uniwersytecie w Syczuanie ogłosili w niedawno opublikowanym badaniu, że udało im się „odwrócić” gromadzenie się zbędnego białka amyloidu beta w mózgach myszy po zaledwie trzech wstrzyknięciach nanocząsteczek.
Beta-amyloid to lepki, samoagregujący fragment białka, który jest głównym składnikiem toksycznych blaszek miażdżycowych gromadzących się w mózgach pacjentów z chorobą Alzheimera. Może zacząć się gromadzić na dziesiątki lat przed wystąpieniem objawów choroby Alzheimera, takich jak utrata pamięci i jasności myślenia.
Dzięki wykorzystaniu nanocząsteczek naukowcy byli w stanie naprawić dysfunkcję „bariery krew-mózg”, która chroni mózg przed toksynami w układzie krwionośnym organizmu, umożliwiając transport blaszki miażdżycowej poza mózg, gdzie może zostać usunięta – wynika z badania opublikowanego w czasopiśmie medycznym Signal Transduction and Targeted Therapy.
Autorzy stwierdzili, że zaledwie godzinę po serii wstrzyknięć nanocząsteczek „zaobserwowaliśmy redukcję ilości beta-amyloidu w mózgu o 50–60%”, dodając, że badana mysz – odpowiadająca 90 latom w przeliczeniu na wiek ludzki i genetycznie zaprogramowana na wysoki poziom beta-amyloidu – wykazywała normalne zachowanie sześć miesięcy po leczeniu, w tym odwrócenie pogorszenia funkcji poznawczych i pamięci.
Wyniki wskazują na „uderzające odwrócenie patologii choroby Alzheimera” i otwierają nową ścieżkę badań, skupiającą się na przywróceniu prawidłowego funkcjonowania niezwykle złożonego układu naczyń krwionośnych mózgu poprzez naprawę bariery krew-mózg, powiedział główny autor, Giuseppe Battaglia, profesor badawczy w Instytucie Katalonii i główny badacz tamtejszej Grupy Biologii Molekularnej.
„Opracowano wiele metod leczenia mających na celu usunięcie beta-amyloidu, lepkiego białka, które gromadzi się w mózgach osób chorych na Alzheimera” – powiedział UPI w komentarzach przesłanych e-mailem. „Niektóre z nich mogą usunąć blaszki, ale samo to nie powstrzymało utraty pamięci ani nie spowolniło wystarczająco postępu choroby.
„Nasza praca wskazuje na inne podejście: zamiast skupiać się wyłącznie na usuwaniu tego, co już uległo uszkodzeniu w mózgu, staramy się naprawić system, który w pierwszej kolejności odpowiada za zdrowie mózgu — jego naczynia krwionośne i barierę ochronną.
„Przywrócenie tej bariery poprawia przepływ krwi, zmniejsza stan zapalny i pomaga mózgowi odzyskać równowagę” – powiedział. „To podejście może skuteczniej spowolnić postęp choroby Alzheimera, lecząc jedną z jej najwcześniejszych i najczęściej pomijanych przyczyn – załamanie się systemu obronnego mózgu”.
Battaglia powiedział, że nanocząsteczki działają jak „lek supramolekularny” mający zdolność „włączania” ważnego białka w barierze krew-mózg, które zazwyczaj działa jako naturalny system oczyszczania organizmu z toksycznych substancji, takich jak beta-amyloid, ale ulega rozpadowi u pacjentów z chorobą Alzheimera.
„Bariera krew-mózg, czyli BBB, to system bezpieczeństwa mózgu: rozległa sieć maleńkich naczyń krwionośnych, które chronią i odżywiają każdy neuron” – wyjaśnił. „Na każdą komórkę mózgową przypada mniej więcej jedna kapilara, która dostarcza tlen i usuwa produkty przemiany materii. Kiedy ten system zawodzi, delikatna równowaga mózgu zostaje zaburzona”.
W chorobie Alzheimera bariera krew-mózg zaczyna zanikać już na wczesnym etapie i jest to jeden z najwcześniejszych objawów ostrzegawczych choroby: ponad 90% pacjentów wykazuje oznaki uszkodzenia naczyń, jeszcze zanim pojawią się problemy z pamięcią. Bariera staje się „nieszczelna” i umożliwia przedostawanie się szkodliwych cząsteczek do mózgu, utrudniając usuwanie produktów przemiany materii i przyspieszając rozwój choroby.
„Nasze badania koncentrują się na pomocy mózgowi w naprawie własnych naczyń krwionośnych i przywróceniu naturalnej funkcji bariery” – powiedział badacz. „Wspierając ten proces regeneracji, odkryliśmy, że zdrowie mózgu poprawia się, a terapie stają się znacznie skuteczniejsze, ponieważ leki docierają do obszarów docelowych, a mózg może lepiej się chronić”.
Potrzeba nowych metod leczenia choroby Alzheimera pozostaje paląca. Prawie co dziewiąty Amerykanin powyżej 65. roku życia cierpi na tę chorobę, podczas gdy w przypadku osób w wieku 85 lat i starszych ryzyko to wynosi jeden do pięciu.
Skupienie się na dysfunkcji BBB w chorobie Alzheimera jest powszechnie uważane za „ogromne znaczenie” zarówno dla wczesnego wykrywania choroby, jak i dogłębnego badania jej mechanizmów. Bariera ta jest niezbędna do filtrowania większych cząsteczek, które mogłyby w przeciwnym razie przedostać się do mózgu przez krwiobieg, zapobiegając w ten sposób przedostawaniu się bakterii, wirusów i substancji toksycznych do mózgu.
Służy również do transportu toksyn, takich jak beta-amyloid, z wnętrza mózgu przez ściśle upakowane komórki, w celu ich usunięcia do krwiobiegu – funkcja ta pozostaje słabo poznana. W zdrowym organizmie bariera krew-mózg wykorzystuje białko receptora sygnałowego o nazwie LRP1, ale u pacjentów z chorobą Alzheimera sygnalizacja LRP1 ulega zaburzeniu.
Nanocząsteczki wykorzystane w niniejszym badaniu wydają się pobudzać proces usuwania LRP1 poprzez naśladowanie białka wiążącego się z blaszką miażdżycową, pomagając w ten sposób „przywrócić naturalną rolę układu naczyniowego jako szlaku usuwania odpadów i przywrócić mu prawidłowe funkcjonowanie”.
Jak powiedział lider tej organizacji non-profit w komentarzu przekazanym UPI, pogłębianie wiedzy na temat roli Better Alzheimer's Association to „ważny i ekscytujący obszar badań”, który zyskał wsparcie ze strony Alzheimer's Association, mimo że wciąż jest w powijakach.
Courtney Kloske, dyrektor ds. zaangażowania naukowego stowarzyszenia, powiedziała, że jej grupa wsparła kilka badań nad BBB, w tym badania mające na celu sprawdzenie, w jaki sposób uszkodzenie BBB może wpływać na postęp choroby, a także prace nad zwiększeniem ilości leków, które mogą przedostać się przez barierę.
„W modelach zwierzęcych prowadzonych jest wiele badań mających na celu znalezienie innowacyjnych metod przekraczania bariery krew-mózg (BBB) w celu zwiększenia efektywności i precyzji dostarczania leków, ale wciąż daleka droga przed nami, zanim technologie te zostaną udowodnione jako bezpieczne i skuteczne u ludzi” – przestrzegła.
Hiszpańsko-chińskie badanie opiera się na badaniach na mysim modelu choroby Alzheimera i chociaż zwierzęce modele choroby są „w pewnym stopniu podobne do sposobu, w jaki choroba Alzheimera postępuje u ludzi, nie odzwierciedlają one dokładnie przebiegu choroby u ludzi” – zauważyła. „Modele są ważne, ponieważ pomagają nam zrozumieć podstawy biologii choroby, ale potrzebujemy badań na reprezentatywnych populacjach, aby w pełni zweryfikować te teorie”.
„Chociaż są to intrygujące odkrycia, konieczne są dalsze badania, aby zrozumieć mechanizmy leżące u podstaw BBB oraz potencjalny wpływ i skutki działania tych związków na osoby chorujące na chorobę Alzheimera lub zagrożone tą chorobą” – powiedział Kloske.



